Uso de componentes y kits de envasado parenteral listos para usar (RTU) para mejorar la eficacia operativa
Robert Popilock
Enfoque heredado y retos
Los productos farmacéuticos parenterales se fabrican siguiendo estrictas directrices de esterilidad mediante procesos asépticos y controles de calidad bien documentados y validados. Estos son ejecutados por personal altamente capacitado que utiliza componentes de envasado primario listos para usar (RTU) (viales de suero, tapones y sellos de aluminio) a menudo preparados en la empresa o en línea. Las agencias reguladoras esperan que los desarrolladores y envasadores de medicamentos garanticen que los componentes cumplen con los controles globales de fabricación estéril fundamentales para su capacidad de suministrar medicamentos inyectables que cumplan con los requisitos de seguridad del paciente, eficacia del medicamento y vida útil. Los desarrolladores y envasadores que optan por procesar internamente los componentes del envase primario se enfrentan a retos relacionados con la garantía de esterilidad y a una carga significativa de costes iniciales y operativos.
Un enfoque simplificado del llenado aséptico
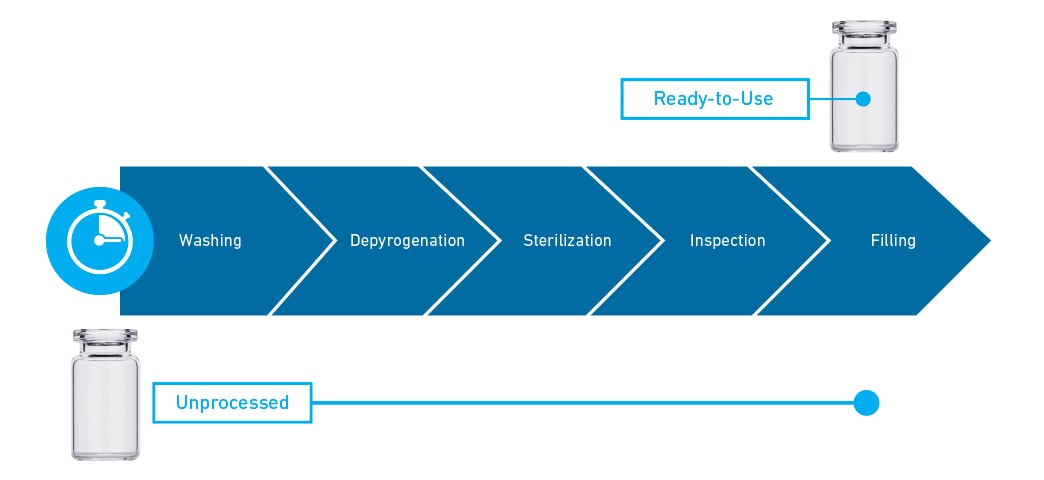
El reciente crecimiento de productos biológicos inyectables personalizados, complejos y de alto valor está impulsando la necesidad de que los laboratorios de investigación y desarrollo de fármacos cualifiquen y utilicen envases RTU para acelerar los plazos de desarrollo y eliminar los riesgos de adopción posteriores. El interés por sustituir el lavado, la despirogenación y la esterilización internos (figura 1) por sistemas de cierre de envases RTU (CCS)1,2 también se debe a la reducción de costes y esfuerzos asociados a la limpieza y esterilización internas o en línea tradicionales, ya que se elimina el complejo diseño de las instalaciones, la inversión en bienes de equipo, los controles y validaciones de procesos y los operarios especializados3.
Figura 1: Limpieza interna tradicional frente a envasado listo para usar (RTU)
Productividad y ahorro de costes
Los componentes de las RTU se preparan para su entrada directa en el núcleo aséptico y van acompañados de documentación controlada por lote que certifica su procesamiento. Esto supone un ahorro estimado del 37% en costes operativos y una reducción total de costes del 80% por la eliminación del equipo de procesado (figura 2)4.
Figura 2: Costes operativos de la limpieza interna frente al envasado listo para usar (RTU)

Ventajas de la cascada
Más allá del coste, muchos fabricantes de medicamentos buscan reducir los riesgos asociados a la implantación de controles de proceso en línea y a la ejecución de las validaciones exigidas por los organismos reguladores internacionales para demostrar la conformidad con las normas de esterilidad5. Los componentes de las RTU están certificados conforme a las normas USP de aplicación inyectable y se envían con certificaciones de trazabilidad de lotes que permiten la entrada directa en el núcleo aséptico. La eliminación de equipos de procesamiento dedicados a la limpieza de partículas, la eliminación de endotoxinas y la esterilidad conserva un valioso espacio operativo para actividades de mayor valor. La eliminación de equipos elimina además los costes asociados a productos químicos, mantenimiento, funcionamiento y reparación.
Conclusión
La industria de los medicamentos inyectables se está preparando para una migración continua desde el procesamiento en línea/en casa, que requiere mucho tiempo, capital y operaciones intensivas, basado en el riesgo, hacia las ventajas racionalizadas y flexibles que ofrece el envasado primario en RTU. Los desarrolladores, los envasadores clínicos y los envasadores comerciales están superando los retos mediante el uso de viales, tapones, precintos y tapas a presión RTU estándar del sector para obtener el coste total de propiedad asociado y las ventajas de cumplimiento normativo. La gama de configuraciones de RTU que ofrece DWK Life Sciences™ satisface requisitos específicos de desarrollo y operativos, beneficiando tanto a los procesos de llenado manual como a los de llenado automatizado. También se prevé que la compatibilidad con los sistemas RABS/aislamiento acelere la adopción de las RTU.
Referencias
- Markarian J. Filling Small Batches, Pharmaceutical Technology Biologics and Sterile Drug Manufacturing eBook. 2021; 2: 14-17. www.pharmtech.com/view/filling-small-batches
- Brooks K. Pharmaceutical Packaging Market Report. Contract Pharma. June 2019. www.contractpharma.com/issues/2019-06-01/view_features/pharmaceutical-packaging-market-trends/
- Challener CA. Prepping Fill/Finish Systems to Ensure Quality Output. BioPharm International. 2020; 33(12): 13-20. www.biopharminternational.com/view/prepping-fill-finish-systems-to-ensure-quality-output
- Prince Sterilization Services LLC. RTU Contract Processing Workflow. 2021.
- Vines M. Parenteral Manufacturing Market Trends. Contract Pharma. March 2015. www.contractpharma.com/issues/2015-03-01/view_features/parenteral-manufacturing-market-trends/
Contenido proporcionado por:



