Síntesis de amidas
Aminación de cloruros o anhídridos de acilo
El acoplamiento directo entre un ácido carboxílico y una amina difícilmente sea una opción adecuada en la química sintética debido al intercambio de protones de ácido/base que compiten. La estrategia más frecuente es la conversión del ácido a una forma activada (es decir, más electrófila) como el cloruro o el anhídrido de acilo. Estas especies reaccionan inmediatamente con las aminas primarias y secundarias y producen la amida correspondiente.
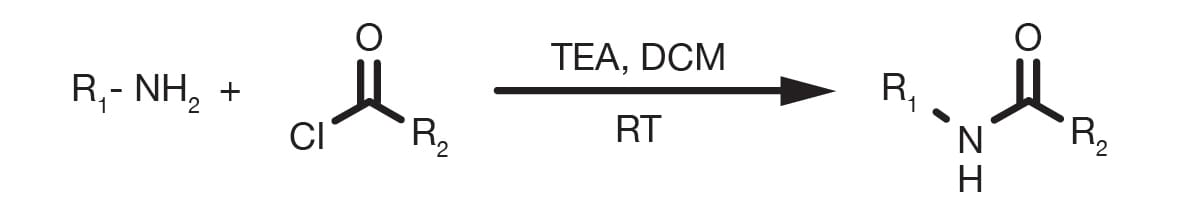
La acilación de aminas mediante cloruro de acilo suele denominarse reacción de Schotten-Baumann, nombre que proviene de sus inventores. Con mayor frecuencia, la reacción comienza rápidamente a temperatura ambiente en disolventes apróticos en presencia de una base adecuada, como por ejemplo, aminas terciarias o piridina. A menudo, se añade una solución acuosa de la base en gotas, que finalmente genera un sistema bifásico. La reacción de Schotten-Baumann y el acoplamiento entre la amina y un anhídrido están mecánicamente relacionados, la única diferencia significativa es el producto derivado del ácido: ácido clorhídrico (HCl) en un caso, un ácido carboxílico en el otro. Ambos requieren una base para dirigir el equilibrio hacia la derecha.
La preparación del cloruro de acilo puede llevarse a cabo in situ mezclando el ácido carboxílico con cloruro de tionilo o cloruro de oxalilo en disolventes apróticos como DCM, THF, o acetato de etilo. Al someter la mezcla a reflujo durante algunas horas, suelen obtenerse conversiones correctas. Es necesario aislar el cloruro de acilo antes de realizar el paso de amidación con la amina.
Métodos derivados de la química péptida (intermediarios de ésteres activos)
Durante las últimas tres décadas se ha logrado un importante avance en la síntesis de las amidas gracias a la investigación en el campo de la síntesis de péptidos. La gran variedad de reactivos de acoplamiento de péptidos disponibles actualmente en el mercado comparte un principio químico fundamental: la síntesis de un éster altamente activo. Aunque muchos de los reactivos de acoplamiento de péptidos fueron específicamente diseñados para una fase sólida automatizada o una síntesis péptida de la solución, en principio pueden usarse las mismas estrategias sintéticas de la síntesis de cualquier amida. Los reactivos más frecuentes pertenecen a dos grupos principales:
- • Carbodiimidas
- • Sales de amonio/uranio o fosfonio de hidroxibenzotriazol
Activación de carbodiimida
Dos de los reactivos más frecuentes de este grupo son diclohexilcarbodiimida (DCC), diisopropilcarbodiimida (DIC) y 1-etil-3- (3-dimetilaminopropil) carbodiimida (EDC). Estos reactivos reaccionan con ácidos carbonílicos para formar una O-acilisourea altamente reactiva que se puede convertir en una amida mediante la reacción con una amina, con alta productividad y tiempos cortos de reacción.
La síntesis de O-acilisoureas se ve beneficiada por el uso de disolventes apolares cuando sea posible (p. ej., DCM), aunque se pueden usar muchos disolventes apróticos apolares.
Las O-acilisoureas se encuentran entre los intermediarios más activos para el acoplamiento de las amidas; sin embargo, pueden racemizarse espontáneamente. Esto debe tenerse en cuenta en la estrategia sintética.
Este también es el motivo por el cual en la síntesis péptida la activación del ácido carboxílico suele realizase en presencia de aditivos de hidroxibenzotriazol que reaccionan rápidamente con el éster activado. En este caso, el paso de activación debe describirse mejor como una activación de DCC/hidroxibenzotriazol de dos pasos.
Este segundo paso de reacción genera otro éster activado que no se racemiza, sino que retiene un nivel suficiente de activación para un acoplamiento eficiente de los péptidos.
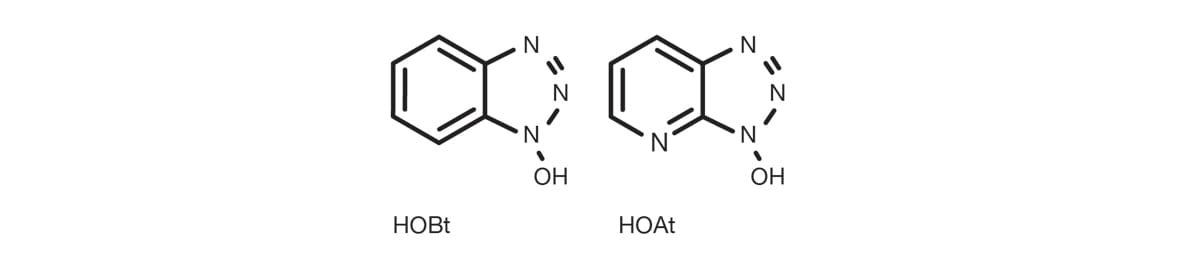
Los triazoles más frecuentes para esta aplicación son 1-hydroxy-benzotriazole (HOBt), y 1-hidroxi-7-aza-benzotriazol (HOAt).
Activación con sales de amonio/uranio y fosfonio de hidroxibenzotriazol
Se logra una estrategia para evitar el proceso de activación de acilos de dos pasos en la química péptida mediante el uso de sales de amonio/uranio o fosfonio de los hidroxitriazoles mencionados anteriormente. De esta manera, es posible evitar por completo el uso de DCC y la formación del intermediario de O-acilisoureas.
HOBt cuenta con una sal de uranio correspondiente llamada HBTU y sus sales de fosfonio comunes se denominan HBTU and its common phosphonium salts are called BOP y PyBOP. Las sales de uranio y fosfonio correspondientes de HOAt son HATU y AOP/PyAOP, respectivamente.
HOBt – HBTU (o TBTU) – BOP o PyBOP
HOBt – HBTU (or TBTU) – BOP or PyBOP
HOAt – HATU – AOP or PyAOP
La reacción directa entre el ácido carboxílico y HATU/AOP/PyAOP o HBTU/BOP/PyBOP ocurre en presencia de una base (generalmente DIEA, diisopropiletilamina) en disolventes orgánicos apróticos polares como DMF, o acetonitrilo.
Estos ésteres activados pueden acoplarse eficazmente con una amina empleando condiciones de reacción similares a las de la reacción de Schotten-Baumann (base, disolvente aprótico, RT).
Protocolos de reacción de referencia
Reacción de Schotten-Baumann:
1.
Prepare una solución de agitación de la amina en DCM; añada una cantidad equimolar de base (p. ej., DIEA), seguida de 1 a 2 equivalentes del cloruro de acilo. Agite a temperatura ambiente durante 8-16 h. Por lo general, la reacción se neutraliza con agua y se obtiene un extracto con DCM u otros disolventes orgánicos según las características de la amida.
2.
Prepare la solución de la amida y la base (equimolar) a 0 °C. Enfríe la mezcla en condiciones de agitación hasta los –75 °C; a continuación, añada el cloruro de acilo. Agite durante 1-6 h, luego neutralice con agua, obtenga un extracto con DCM y proceda con la purificación del producto.
Método de carbodiimida:
Prepare una solución del ácido en DMF añadiendo aproximadamente 2 o 3 equivalentes de la base. Enfríe la solución a 0 °C y añada 2 equivalentes de DCC o EDC. Agite a temperatura ambiente durante 30-60 min; a continuación, diluya con agua y obtenga un extracto con un disolvente orgánico de acuerdo con las propiedades del producto de amida. Proceda con la purificación del producto.
HATU/HBTU
Prepare una solución del ácido en DMF a 0 °C; a continuación, añada 2 equivalentes de HATU (550 mg, 1,4 mmol) y 3 equivalentes de la base (p. ej., DIEA o TEA). Finalmente, añada un pequeño exceso de la amina (en comparación con el ácido) y agite a temperatura ambiente durante 30-60 min. Diluya con agua y obtenga un extracto con un disolvente orgánico de acuerdo con las propiedades del producto de amida. Proceda con la purificación del producto.
El protocolo de referencia es el mismo en caso de usar otros activadores, como AOP, PyBOP, BOP, etc.
Si se utiliza HBTU, el protocolo es similar; sin embargo, a menudo es necesario aumentar la temperatura de la reacción y algunos autores notifican condiciones de reflujo y tiempos de conversión ligeramente más prolongados, de hasta 2 o 3 horas.
Uso combinado de carbodiimida e hidroxibenzotriazol
Prepare una solución del ácido (700 mg, 3,2 mmol) en DMF (10 ml); añada 3 equivalentes de la base (p. ej., DIEA, NH4Cl o TEA) al tiempo que enfría la reacción a 0 °C. Trate la mezcla con 2 equivalentes de etilcarbodiimida (u otra carbodiimida) y 2 equivalentes de HOBt (o HOAt), finalmente, añada 1,5 equivalentes de la amina. Agite a temperatura ambiente durante 30-60 min. Neutralice con agua y obtenga un extracto con un disolvente orgánico de acuerdo con las propiedades del producto de amida. Proceda con la purificación del producto.
Ejemplos
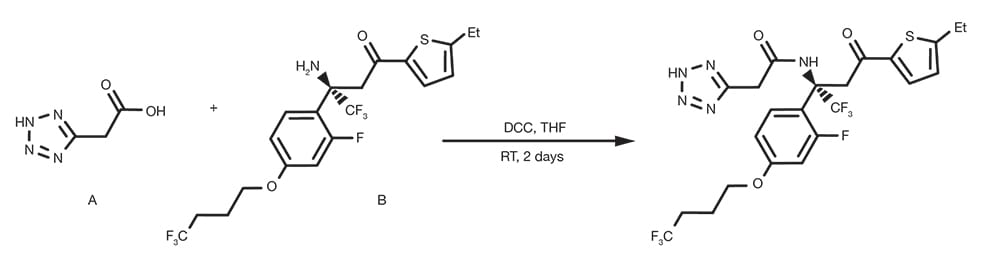
Referencia de patente: WO2015191681
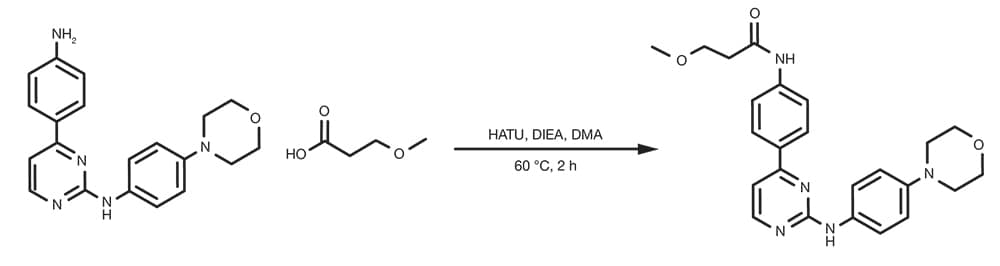
Referencia de patente: WO2015129926
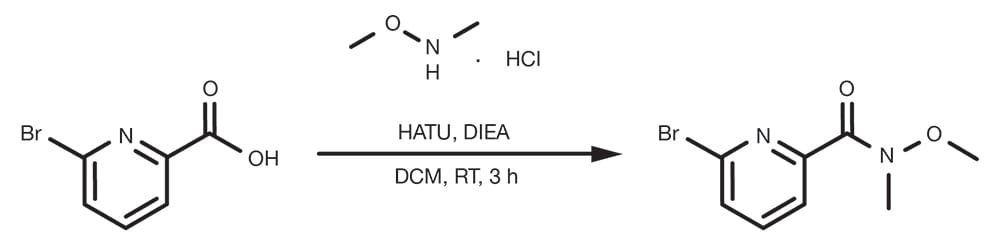
Referencia de patente: WO2015140133
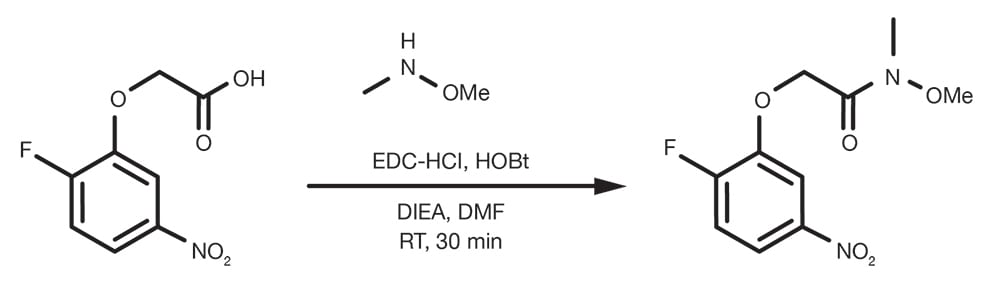
Referencia de patente: WO2014149164
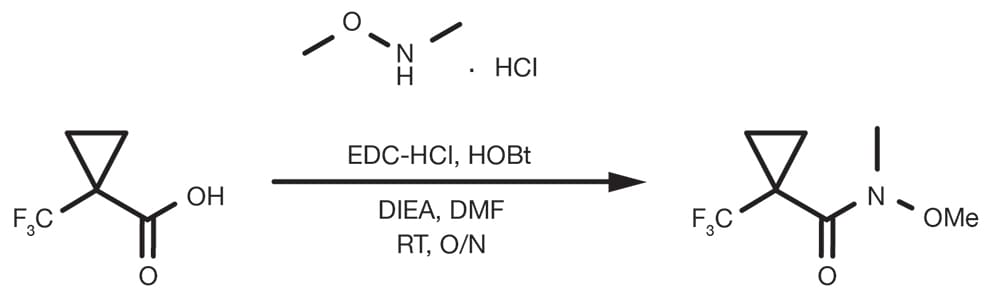
Referencia de patente: WO2015129926
Referencias bibliográficas clave
- Schotten, C. Berichte der deutschen chemischen Gesellschaft. 1884, 17, 2544. doi:10.1002/cber.188401702178.
- Baumann, E. Berichte der deutschen chemischen Gesellschaft. 1886, 19, 3218. doi:10.1002/cber.188601902348.
- Emil Fischer Berichte der deutschen chemischen Gesellschaft. 1903, 36, 2982–2992. doi:10.1002/cber.19030360356.
- Jaradat, Da’san M. M. "Thirteen decades of peptide synthesis: key developments in solid phase peptide synthesis and amide bond formation utilized in peptide ligation". Amino Acids. 2017, 50 (1): 39-68. doi:10.1007/s00726-017-2516-0. ISSN 0939-4451
- El-Faham A, Albericio F. "Peptide coupling reagents, more than a letter soup". Chemical Reviews. 2011, 111, 6557-602. doi:10.1021/cr100048w
Selección del producto
Disolventes:
Tratamiento de la reacción:
CONSULTE TODOS NUESTROS DISOLVENTES: CONTAMOS CON MÁS DE 1000 ALTERNATIVAS
Ingredientes y aditivos básicos:
Tratamiento de la reacción:
USE LA BARRA DE BÚSQUEDA SITUADA EN LA PARTE SUPERIOR DE LA PÁGINA PARA REALIZAR BÚSQUEDAS ESPECIFICAS POR NOMBRE DE PRODUCTO O NÚMERO CAS
Agentes de activación:
1-etil-3-(3-dimetilaminopropil)carbodiimida (EDC)
1-[Bis(dimetilamino)metileno]-1H-1,2,3-triazolo[4,5-b]piridinio 3-óxido hexafluorofosfato (HATU)
N,N,N”,N”-tetrametil-O-(1H-benzotriazol-1-yl)uranio hexafluorofosfato
O-(benzotriazol-1-yl)-N,N,N',N'-tetrametiluronio hexafluorofosfato (HBTU)
(Benzotriazol-1-yloxy)tris(dimetilamino)fosfonio hexafluorofosfato (BOP))
(Benzotriazol-1-yloxy)tripirrolidinofosfonio hexafluorofosfato (PyBOP)
Tris(dimetilamino)(3H-1,2,3-triazolo[4,5-b]piridina-3-yloxy)fósforo hexafluorofosfato (AOP)
(7-azabenzotriazol-1-yloxy)tripirrolidinofosfonio hexafluorofosfato (PyAOP)
USE LA HERRAMIENTA DE BÚSQUEDA DE ESTRUCTURAS QUÍMICAS PARA BUSCAR EL COMPONENTE BÁSICO QUE NECESITA
Componentes básicos:
Alquilo o (het) cloruros de acilo aromáticos:
Cloruro de isoxazol-5-carbonilo
Alquilo o (het) ácidos carboxílicos aromáticos:
Ácido 3,5-dimetoxi-4-metilbenzoico
Otros ácidos carboxílicos (más de 5000 artículos)
Alquil nitrilos (amidas de la hidrólisis de nitrilo):
Cetonas cíclicas saturadas (para la amidación de Sheppard para dar lactamas):
N- (etoxicarbonil) nortropinona
Aril alquil cetonas:
Amoniaco (solución en metanol)
Aminas: